세포 분열의 시계: 2001년 노벨 생리의학상 – 세포 주기 조절의 발견
2001년 노벨 생리의학상은 세포 주기의 조절 메커니즘을 발견한 릴랜드 하트웰(Leland H. Hartwell), 폴 너스(Sir Paul M. Nurse), 티모시 헌트(Tim Hunt)에게 수여되었다. 이 세 명의 과학자는 효모부터 인간까지 모든 진핵 생물에서 공통적으로 작동하는 세포 주기 조절의 분자적 원리를 규명하여 생명 과학의 핵심 영역에 중대한 기여를 했다. 이들의 발견은 암과 같은 세포 증식 질환의 병태 생리를 이해하고 치료 방법을 개발하는 데 필수적인 기반을 제공하였다.
세포 분열의 핵심인 세포 주기
모든 유기체는 세포 분열을 통해 증식하는 세포로 구성되어 있다. 성인 인간은 약 1억 개의 세포를 가지고 있으며, 모두 수정란이라는 단일 세포에서 유래한다. 성인의 경우 죽어가는 세포를 대체하기 위해 지속적으로 분열하는 세포도 많다. 세포가 분열하기 전에는 세포의 크기가 커지고 염색체가 복제되며, 두 딸 세포에 염색체가 정확하게 분포되어야 한다. 이 복잡한 과정은 세포 주기라는 정교한 프로그램에 의해 조절된다.
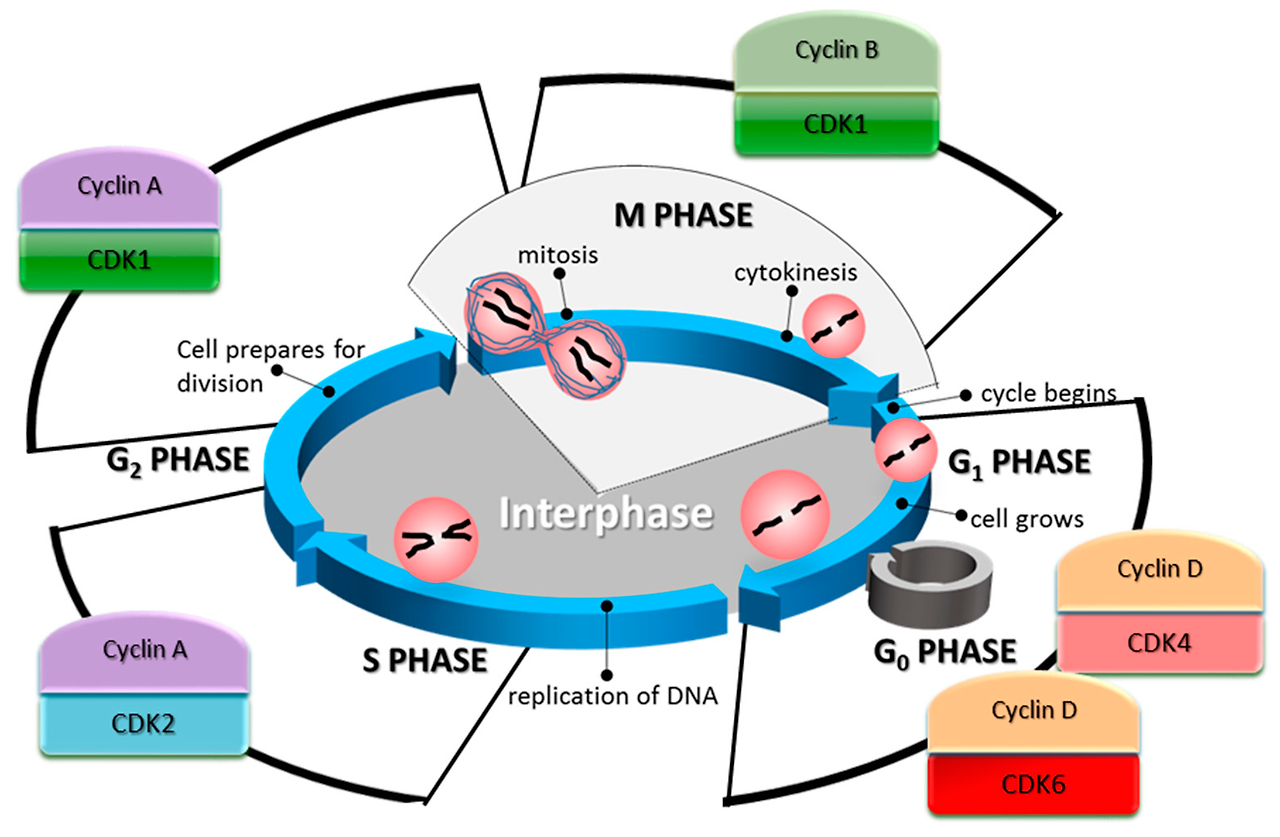
세포 주기는 G1, S, G2, M 단계로 구성된다. G1 단계에서는 세포가 성장하고, S 단계에서는 DNA 복제가 이루어진다. G2 단계는 복제가 완료된 DNA를 점검하는 시기이며, M 단계에서는 유사 분열을 통해 세포가 둘로 나뉜다. 이 과정의 정확성은 생물의 생존과 직결되며, 오류는 종종 암과 같은 질병으로 이어진다. 특히 세포 주기에서 어떤 시점에 어떤 유전자가 발현되고 억제되어야 하는지를 정확히 조절하는 것이 핵심이며, 이 정교한 시스템이 깨질 경우 다양한 질환의 원인이 될 수 있다.
릴랜드 하트웰의 유전자와 체크포인트 발견
하트웰은 세포 주기 조절에 관여하는 유전자를 효모 모델에서 체계적으로 확인했다. 그는 특히 세포 주기의 시작을 담당하는 유전자인 "시작(start)"을 발견하였고, 세포 주기 중 DNA 손상 시 일시적으로 세포 주기를 정지시키는 "체크포인트(checkpoint)" 개념을 처음으로 제시했다. 이 발견은 DNA 복구가 완료되지 않은 상태에서 세포 분열이 진행되어 유전적 이상이 누적되는 것을 방지하는 생명 유지 시스템의 핵심 원리로 이해되었다.
이 체크포인트 시스템은 암세포에서 비정상적으로 작동하거나 아예 무력화된 경우가 많다. 따라서 하트웰의 발견은 암 진단 및 예후 분석, 그리고 새로운 치료 전략 수립에 중요한 이론적 기반을 제공하였다.
폴 너스와 CDK 유전자
폴 너스는 또 다른 효모 모델인 쉬조사카로미세스 폼베에서 cdc2 유전자를 발견했다. 이 유전자는 G2에서 M기로의 전이를 조절하며, G1에서 S기로의 전환도 관여한다. 놀라운 점은 인간을 포함한 모든 진핵생물에서 이 유전자가 유사한 기능을 수행한다는 것이다. 인간에서는 이 유전자가 CDK1(사이클린 의존성 키나아제 1)로 명명되었다. CDK는 인산화 반응을 통해 다른 단백질을 조절하며, 세포 주기의 각 단계를 정확하게 통과하도록 돕는다.
너스의 연구는 세포 분열의 정확성과 생존율을 결정짓는 핵심 유전자의 보편성과 진화적 보존성을 강조하였으며, 이후 여러 유형의 CDK와 사이클린 조합이 어떻게 작동하는지에 대한 다양한 연구를 촉진시켰다. CDK1 외에도 CDK2, CDK4, CDK6 등의 단백질들은 특정 세포 주기 단계에서 각각의 기능을 수행하며, 이들은 다양한 암세포에서 비정상적으로 활성화되거나 발현량이 증가되어 있는 경우가 많다.
티모시 헌트와 사이클린의 발견
티모시 헌트는 성게의 난세포를 관찰하는 과정에서 세포 주기 동안 주기적으로 생성되고 파괴되는 단백질, 즉 사이클린을 발견하였다. 사이클린은 CDK와 결합하여 그 활성을 조절하고, 세포 주기에서 적절한 시점에 특정 반응을 유도한다. 이처럼 사이클린과 CDK는 서로 상호작용하며 세포 주기의 추진 엔진이 된다. 헌트는 이후 다른 생물에서도 사이클린이 존재한다는 사실을 밝혀내며, 이 메커니즘이 진화적으로 보존된 시스템임을 입증했다.
사이클린의 정교한 조절은 세포가 환경 변화에 적응하고 외부 자극에 반응하는 메커니즘과도 연결된다. 또한 헌트의 발견은 세포 주기를 인위적으로 조절하여 세포 분열을 억제하거나 촉진하는 약물 개발의 단초를 제공하였다. 예컨대, 특정 사이클린을 억제하는 방식은 암세포의 증식을 막는 새로운 치료법으로 발전 중이다.
진핵 세포와 유전 정보의 정교한 통제
진핵 세포는 20억 년 전 지구상에 등장하였으며, 각 세포는 핵 내 염색체에 유전 정보를 담고 있다. 인간의 경우, 세포 하나하나에는 46개의 염색체(23쌍)가 존재하고, 그 속에는 전체 유전체 정보가 들어 있다. 이런 정교한 정보 전달과 분열 과정에서 오류가 발생하면 생명 유지에 큰 위협이 될 수 있다. 세포 주기의 정밀한 조절은 유전 정보의 정확한 복제와 분배를 보장하는 핵심 요소이다.
세포 주기 조절 메커니즘을 이해함으로써 과학자들은 이제 암세포의 비정상적인 성장과 분열, 그리고 염색체의 불균형 분포 같은 현상을 설명할 수 있게 되었다. 예를 들어, 종양 세포에서는 CDK나 사이클린의 발현이 비정상적으로 증가하거나, 반대로 종양 억제 단백질이 제대로 작동하지 않을 수 있다. 이러한 지식은 향후 진단과 치료, 특히 CDK 억제제와 같은 표적 치료제 개발에 핵심적 기반이 된다.
생명과학과 의학에 미친 영향
세포 주기 연구는 암 이외에도 다양한 생리적, 병리적 현상을 이해하는 데 필수적이다. 예를 들어, 조직 재생, 줄기세포 분화, 면역 세포 활성화, 신경세포 재생 등 여러 과정이 세포 주기 조절에 기반하고 있다. 특히 세포 분열이 활발히 일어나는 조직에서의 CDK 억제제 응용은 유망한 치료법으로 주목받고 있으며, 현재 여러 제약회사가 CDK 억제제를 활용한 항암제 개발에 박차를 가하고 있다.
2001년 노벨 생리의학상 수상자들의 발견은 생물학의 기본 원리를 밝히는 동시에 의학적 응용 가능성을 제시함으로써 기초 연구와 임상 연구 간의 다리를 놓는 결정적 계기가 되었다. 세포 주기 조절이라는 개념은 더 이상 이론적인 지식에 그치지 않고, 다양한 질환의 진단 및 치료 전략에 실질적인 영향을 미치고 있다. 이들의 공헌은 생명과학 분야의 지속적인 발전과 질병 극복을 위한 노력에 중요한 전환점을 제공한 위대한 업적이라 할 수 있다.
'생명과학' 카테고리의 다른 글
| 2006년 노벨 생리의학상 – RNA 간섭(RNAi)의 발견과 의학적 혁신 (2) | 2025.08.07 |
|---|---|
| 2004년 노벨 생리의학상 – 후각의 과학을 열다: 냄새를 인식하는 유전자 지도 (6) | 2025.08.06 |
| 2003년 노벨 생리의학상 – 인체를 투시하다: MRI 기술의 혁명 (3) | 2025.08.06 |
| 2002년 노벨 생리의학상- 프로그램된 세포 죽음의 열쇠를 푼 발견 (4) | 2025.08.06 |
| 2000년 노벨 생리의학상: 신경 신호의 비밀을 밝히다 (2) | 2025.08.06 |
| 1999년 노벨 생리의학상 – 단백질의 “주소 태그” (2) | 2025.08.06 |
| 1998년 노벨 생리의학상 -혈관 확장의 분자 메커니즘: 산화질소(NO)의 발견 (1) | 2025.08.05 |
| 1997년 노벨 생리의학상-새로운 감염 원리의 도래: 프리온 개념의 등장 (0) | 2025.08.05 |



